Back سلفولان Arabic سولفولان AZB Sulfolan Czech Sulfolan German Sulfolane English سولفولان Persian Sulfolaani Finnish Sulfolane French スルホラン Japanese Sulfolaan Dutch
| Solfolano | |
|---|---|
| Nome IUPAC | |
| 1λ6-Tiolano-1,1-dione | |
| Nomi alternativi | |
| tetrametilensolfone 1,1-diossitiolano diossido di 1,1-tetraidrotiofene bondelano A solfone ciclico di tetrametilene NSC 46443 diossido di S,S-tetraidrotiofene diossido di tiaciclopentano diossido di 1,1-tiolano diossido di tiofano diossido di 1,1-tetraidrotiofano ciclobutilsolfone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C4H8O2S |
| Massa molecolare (u) | 120,17 |
| Aspetto | solido o liquido incolore |
| Numero CAS | |
| Numero EINECS | 204-783-1 |
| PubChem | 31347 |
| SMILES | C1CCS(=O)(=O)C1 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,261, liquido |
| Indice di rifrazione | 1,482 - 1,485 |
| Solubilità in acqua | completa |
| Temperatura di fusione | 27,5 °C (300,65 K) |
| Temperatura di ebollizione | 285 °C (558,15 K) |
| Tensione di vapore (Pa) a 303 K | 3,5 (30 °C) |
| Viscosità cinematica (m2/s a 30 °C) | 10,34 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 1941 mg/kg - Orale (ratti) 4009 mg/kg - Dermale (conigli) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 165 °C (438,15 K) |
| Temperatura di autoignizione | 528 °C (801,15 K) |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 |
| Consigli P | ---[1] |
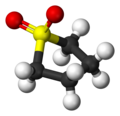
Il solfolano o tetrametilensolfone[2] è un solfone[3] ciclico, un composto organico dello zolfo esavalente, avente formula semistrutturale (CH2)4SO2.
A 25 °C e pressione ambiente è un solido cristallino incolore che però già a 27,5 °C fonde in un liquido incolore di consistenza oleosa e altobollente (285 °C).[4] È importante come solvente in quanto è stabile chimicamente anche alle alte temperature, è molto polare ed è solubile in acqua in ogni proporzione, come pure in svariati solventi organici polari e meno polari, tranne negli idrocarburi alifatici e pochi altri, nei quali è solubile solo parzialmente.[5][4] Il fatto che sia liquido a temperatura quasi ambiente lo rende a volte preferibile al dimetilsolfone, che ha caratteristiche chimiche molto simili, ma che invece fonde solo a 109 °C.
- ^ Sigma Aldrich; rev. del 16.05.2014
- ^ R. Fusco, G. Bianchetti e V. Rosnati, Composti solforati, in CHIMICA ORGANICA, volume primo, L. G. Guadagni, 1974, pp. 734-739.
- ^ Michael B. Smith e Jerry March, MARCH’S ADVANCED ORGANIC CHEMISTRY, 6ª ed., 2007, p. 53, ISBN 978-0-471-72091-1.
- ^ a b (EN) PubChem, Sulfolane, su pubchem.ncbi.nlm.nih.gov. URL consultato il 2 aprile 2023.
- ^ I. L. Finar, ORGANIC CHEMISTRY The fundamental principles, Fourth Edition, Longmans, 1963, p. 338.
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search